bihar board 9th class science notes | परमाणु की संरचना
bihar board 9th class science notes | परमाणु की संरचना
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 53)
प्रश्न 1. केनार किरणें क्या हैं?
उत्तर-1886 ई. में गोल्डस्टीन ने धनावेशित विकिरण की खोज की जिनका नाम उन्होंने
‘केनार रे’ दिया।
प्रश्न 2. यदि किसी परमाणु में एक इलेक्ट्रॉन और एक प्रोटॉन है, तो इसमें कोई
आवेश होगा या नहीं?
उत्तर-कोई आवेश नहीं होगा क्योंकि प्रोटॉन का आवेश +1 इलेक्ट्रॉन के आवेश -1 विपरीत
तथा बराबर है।
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 56)
प्रश्न 1. परमाणु उदासीन है, इस तथ्य को टॉमसन के मॉडल के आधार पर स्पष्ट
कीजिए।
उत्तर-1899 में टॉमसन ने प्रस्तावित किया कि-
(i) परमाणु एक धनात्मक क्षेत्र से बना है जिसमें ऋणात्मक कण इलेक्ट्रॉन यहाँ-वहाँ
विखरे हुए हैं।
(ii) परमाणु के धनात्मक और ऋणात्मक आवेश एक-दूसरे को संतुलित अथवा काट देते
हैं, इसीलिए परमाणु उदासीन होता है।
प्रश्न 2. रदरफोर्ड के परमाणु मॉडल के अनुसार, परमाणु के नाभिक में कौन-सी
अवपरमाणुक कण विद्यमान हैं ?
उत्तर-प्रोटान (धनावेशित) होता है।
प्रश्न 3. तीन कक्षाओं वाले बोर के परमाणु मॉडल का चित्र बनाइए।
उत्तर-
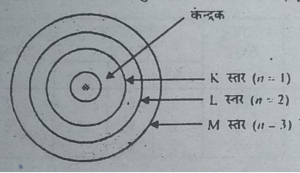
प्रश्न 4. क्या अल्फा कणों का प्रकीर्णन प्रयोग सोने के अतिरिक्त दूसरी धातु की पन्नी
से संभव होगा?
उत्तर-सोना सर्वाधिक आघातवर्ध्य धातु है, और इसीलिए अल्फा-कणों के प्रथम तल के
परमाणुओं से टकराने की संभावना अधिक होती है। साथ ही, सोना सबसे कम क्रियाशील धातु
है। यदि सोने के अलावा किसी अन्य धातु का उपयोग किया जाए, तो हो सकता है कि वह धातु
अल्फा-कणों के साथ अभिक्रिया करे अथवा धातु के कम आघातवर्ध्य होने के कारण अल्फा-कण उसकी मोटी पन्नी के परमाणुओं से टकरा न पाएँ।
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 56)
प्रश्न 1. परमाणु के तीन अवपरमाणुक कणों के नाम लिखें।
उत्तर-परमाणु के तीन अवपरमाणुक कण हैं-
(i) इलेक्ट्रॉन, (ii) प्रोटॉन और (iii) न्यूट्रॉन।
प्रश्न 2 हीलियम परमाणु का परमाणु द्रव्यमान 4u है और उसके नाभिक में दो प्रोटॉन
होते हैं। इसमें कितने न्यूट्रॉन होंगे?
उत्तर-दो न्यूट्रॉन होंगे।
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 57)
प्रश्न 1. कार्बन और सोडियम के परमाणुओं के लिए इलेक्ट्रॉन-वितरण लिखिए।
उत्तर-
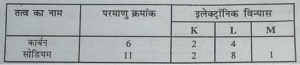
प्रश्न 2. अगर किसी परमाणु का Kऔर Lकोश भरा है, तो उस परमाणु में इलेक्ट्रॉनों
की संख्या क्या होगी?
उत्तर-10 इलेक्टॉन (2+8)।
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 58)
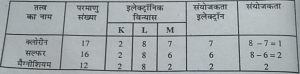
प्रश्न-क्लोरीन, सल्फर और मैग्नीशियम की परमाणु संख्या से आप इनकी संयोजकता
कैसे प्राप्त करेंगे?
उत्तर-तत्व की परमाणु संख्या से इसका इलेक्ट्रॉनिक विन्यास का पता चलता है और
संयोजकता इलेक्ट्रॉन परमाणु संख्या में से संयोजकता इलेक्ट्रॉन घटाने पर उसकी संयोजकता
निकालते हैं।
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 59)
प्रश्न 1. यदि किसी परमणु में इलेक्ट्रॉनों की संख्या 8 है और प्रोटानों की संख्या भी
8 है तब,
(a) परमाणु की परमाणुक संख्या क्या है?
(b) परमाणु का क्या आवेश है?
उत्तर-(i) परमाणु संख्या = प्रोटानों की संख्या =8
(ii) प्रोटानों की संख्या = 8
धनात्मक आवेश = 8
इलेक्ट्रॉनों की संख्या = 8
ऋणात्मक आवेश = 8
कुल आवेश =+8+8(-8)=0
प्रश्न 2. प्रश्न 108 के उत्तर में दी गई सारणी की सहायता से ऑक्सीजन और
सल्फर-परमाणु की द्रव्यमान संख्या ज्ञात कीजिए।
उत्तर-द्रव्यमान संख्या = प्रोटॉन की संख्या + न्यूट्रॉनों की संख्या
ऑक्सीजन की द्रव्यमान संख्या =8+8=16
सल्फर की द्रव्यमान संख्या =16+16=32
पाठ्य पुस्तकीय प्रश्नों के उत्तर (पृष्ठ 60)
प्रश्न 1. चिह्न H.D और T के लिए प्रत्येक में पाए जाने वाले तीन अवपरमाणुक
कणों को सारणीबद्ध कीजिए।
उत्तर-H,D और T हाइड्रोजन के समस्थानिक होते हैं।
अवपरमाणु कणों की सारणी
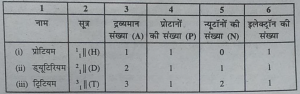
प्रश्न 2. समस्थानिक और समभारिक के किसी एक युग्म का इलेक्ट्रॉनिक विन्यास
लिखिए।

अभ्यास
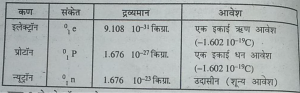
प्रश्न 1. इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन के गुणों की तुलना कीजिए।
उत्तर-
प्रश्न 2. जे. जे टॉमसन के परमाणु मॉडल की क्या सीमाएँ हैं?
उत्तर-हालाँकि टॉमसन के परमाणु संरचना मॉडल ने परमाणु की उदासीन प्रकृति की
भली-भांँति व्याख्या दी, परंतु अन्य वैज्ञानिकों द्वारा किए गए प्रयोगों के निष्कर्षों को यह मॉडल
नहीं दर्शा पाया।
प्रश्न 3. रदरफोर्ड के परमाणु मॉडल की क्या सीमाएंँ हैं ?
उत्तर-रदरफोर्ड के परमाण्विक मॉडल की मुख्य कमी यह थी कि इससे परमाणु के
स्थायित्व का पता नहीं चलता।
जब कोई आवेशित कण त्वरित होता है, तो वह ऊर्जा को विकिरित करता है। विकिरण
के इस उत्सर्जन द्वारा इलेक्ट्रॉन में ऊर्जा की कमी होगी, जिसके कारण उसकी कक्षा के आकार
का संकुचन होगा। फलस्वरूप, कुछ ही समय में इलेक्यन नाभिक से टकरा जाएगा। रदरफोर्ड यह नहीं समझा पाए कि वास्तव में ऐसा क्यों नहीं होता।
प्रश्न 4. बोर के परमाणु मॉडल की व्याख्या कीजिए।
उत्तर-डैनिश वैज्ञानिक नील्स बोर ने 1912 ईस्वी में एक परमाण्विक मॉडल प्रस्तावित किया,
जिसे बोर परमाण्विक मॉडल कहा जाता है। बोर परमाण्विक मॉडल की मूल अवधारणाएंँ इस
प्रकार हैं-
(i) एक परमाणु में, इलेक्ट्रॉन नाभिक के इर्द-गिर्द एक निश्चित चक्रीय पथ पर घूमते हैं।
ये चक्रीय पथ इलेक्ट्रॉन कक्ष या ऑर्बिट (Orbit) कहलाते हैं। इन्हें ऊर्जा स्तर भी कहते हैं।
(ii) प्रत्येक इलेक्ट्रॉन कक्ष एक निश्चित ऊर्जा से युक्त होता है।
(iii) इलेक्ट्रॉन कक्ष या कर्जा स्तरों को (चित्र 4.10) 1.2.3…….या K.L.M…….आदि
से अंकित करते हैं। ये पूर्णांक 1.2.3.4……. को कक्षों की क्वान्टम (quantum) संख्या कहते हैं।
(iv) एक इलेक्ट्रॉन केवल निश्चित व आवश्यक ऊर्जा को खो सकता है या प्राप्त कर सकता
है।
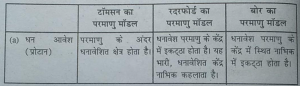
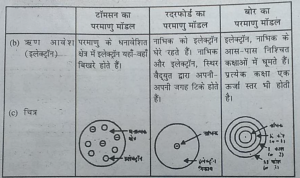
प्रश्न 5. इस अध्याय में दिए गए सभी परमाणु मॉडलों की तुलना कीजिए।
उत्तर-
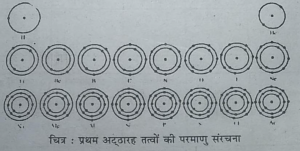
प्रश्न 6. पहले अठारह तत्त्वों के विभिन्न कक्षों में इलेक्ट्रॉन वितरण के नियम को
लिखिए।
उत्तर-किसी परमाणु में विभिन्न ऊर्जा स्तरों (इलेक्ट्रॉन कक्षों) में इलेक्ट्रॉनों के वितरण के
लिए बोर तथा बरी योजना निम्न नियमों पर आधारित है-

(ii) बाह्यतम कक्ष (जिसे संयोजकता कक्ष भी कहते हैं) में अधिकतम 8 इलेक्ट्रॉन हो सकते
हैं और उससे पूर्व वाले कक्ष में अधिकतम 18 इलेक्ट्रॉन हो सकते हैं।
(iii) यह आवश्यक नहीं है कि किसी कक्ष में इलेक्ट्रॉनों की संख्या उससे अग्रिम कक्ष में
इलेक्ट्रॉन भरने से पूर्ण हो जाए।
प्रश्न 7. सिलिकॉन और ऑक्सीजन का उदाहरण देते हुए संयोजकता की परिभाषा
दीजिए।
उत्तर-किसी तत्व के परमाणु की संयोगात्मक क्षमता को उसकी संयोजकता कहते हैं।
परमाणु अपने बाह्यतम कोश को पूर्ण करने के लिए जितने इलेक्ट्रॉन खोता, पाता या बाँटता है,
वही उसकी संयोजकता कहलाती हैं।

ऑक्सीजन को संयोजकता 2 है क्योंकि वह 2 इलेक्ट्रॉन प्राप्त कर अपना बाह्यतम कोश पूर्ण
कर सकता है। सिलिकन की संयोजकता 4 है क्योंकि वह 4 इलेक्ट्रॉन खोकर, पाकर या बाँटकर
अपना बाह्यतम कोश पूर्ण कर सकता है।
प्रश्न 8. उदाहरण के साथ व्याख्या कीजिए-परमाणु संख्या, द्रव्यमान संख्या, समस्थानिक
और समभारिक समस्थानिकों के कोई दो उपयोग लिखिए।
उत्तर-(i) किसी तत्व के एक परमाणु के नाभिक में मौजूद प्रोट्रॉनों की संख्या को उसकी
परमाणु संख्या कहते हैं।
हाइड्रोजन के लिए, Z= 1 क्योंकि हाइड्रोजन परमाणु के नाभिक में केवल एक प्रोटॉन होता है।
कार्बन के लिए Z= 6 क्योंकि कार्बन परमाणु के नाभिक में 6 प्रोटान होते हैं।
(ii) किसी तत्व के एक परमाणु के नाभिक में उपस्थित प्रोटॉनों और न्यूट्रॉनों की कुल
संख्या उसको द्रव्यमान संख्या कहलाती है। उदाहरण के लिए,
कार्बन की द्रव्यमान संख्या 12 है क्योंकि उसमें 6 प्रोटान और 6 न्यूट्रॉन होते हैं (6+6 =
12)। इसी प्रकार, ऐलुमिनियम की द्रव्यमान संख्या 27 (13 प्रो. +14 न्यू.) होती है।
(iii) किसी तत्व के ऐसे परमाणु जिनकी परमाणु संख्या समान हो परन्तु द्रव्यमान संख्या
भिन-भिन हो, उस तत्व के समस्थानिक कहलाते हैं।
समस्थानिकों को निम्न प्रकार भी परिभाषित किया जा सकता है-
‘किसी तत्व के परमाणु जिनमें प्रोटॉनों की समान संख्या हो परन्तु न्यूट्रॉनों की संख्या भिन्न
हो, उस तत्व को समस्थानिक कहते हैं।’
(i) हाइड्रोजन के तीन समस्थानिक होते हैं-

(ii) क्लोरीन के दो समस्थानिक होते हैं-
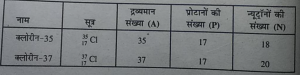
(iii) तत्वों के ऐसे परमाणु जिनकी द्रव्यमान संख्या तो एक हो परंतु परमाणु संख्या भिन्न
हो, उन तत्वों को समभारिक परमाणु कहते हैं। उदाहरण के लिए,
समस्थानिकों के कुछ उपयोग हैं-
(i) यूरेनियम का एक समस्थानिक परमाणु रिएक्टर में ईंधन के रूप में उपयोग किया जाता है।
(ii) कोबाल्ट का एक समस्थानिक कैंसर के इलाज में प्रयुक्त होता है।
(iii) आयोडीन का एक समस्थानिक घेघा रोग के इलाज में प्रयुक्त होता है।
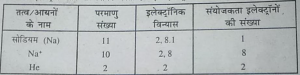
प्रश्न 9. Na+ के पूरी तरह से भरे हुए K व L कोश होते हैं-व्याख्या कीजिए।
उत्तर-इलेक्ट्रॉन खोने से धनायन बनता है। एक इलेक्ट्रॉन खोने से Na+ बनता है।



प्रश्न 12. यदि तत्व का 2=3 हो तो तत्व की संयोजकता क्या होगी? तत्व का नाम
भी लिखिए।
उत्तर-तत्व की परमाणु संख्या Z= 3
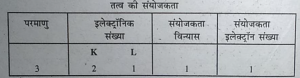
तत्व का नाम = लीथियम।
प्रश्न 13. दो परमाणु स्पीशीज के केंद्रकों का संघटन नीचे दिया गया है-

x और Y की द्रव्यमान संख्या ज्ञात कीजिए। इन दोनों स्पीशीज में क्या संबंध है?
उत्तर-द्रव्यमान संख्या = प्रोटॉनों की संख्या + न्यूट्रॉनों की संख्या
xकी द्रव्यमान संख्या =6+6 = 12
Yकी द्रव्यमान संख्या =6+8= 14
परमाणु संख्या = प्रोटॉनों की संख्या
x की परमाणु संख्या = 6
Y की परमाणु संख्या =6
चूँकि X और Y की परमाणु संख्या एक है किंतु द्रव्यमान संख्या भिन्न है, इसीलिए ये दोनों
समस्थानिक हैं।
प्रश्न 14. निम्नलिखित वक्तव्यों में गलत के लिए F और सही के लिए T लिखें।
(a) जे. जे. टॉमसन ने यह प्रस्तावित किया था कि परमाणु के केंद्रक में केवल
न्यूक्लीयॉन्स होते हैं।
(b) एक इलेक्ट्रॉन और प्रोटॉन मिलकर न्यूट्रॉन का निर्माण करते हैं इसलिए यह
अनावेशित होता है।
1
(c) इलेक्ट्रॉन का द्रव्यमान प्रोटॉन से लगभग ———– गुणा होता है।
2000
(d) आयोडीन के समस्थानिक का इस्तेमाल टिंक्चर आयोडीन बनाने में होता है।
इसका उपयोग दवा के रूप में होता है।
उत्तर-(a). (b). (c). (d) x. (e) √ I
प्रश्न संख्या 15, 16 और 17 में सही के सामने (√) का चिह्न और गलत के सामने (x)
का चिह्न लगाइए।
प्रश्न 15. रदरफोर्ड का अल्फा कण प्रकीर्णन प्रयोग किसकी खोज के लिए
उत्तरदायी था-
(a) परमाणु केंद्रक
(b) इलेक्ट्रॉन
(c) प्रोटॉन
(d) न्यूट्रॉन उत्तर-(a) परमाणु केंद्रक।
प्रश्न 16. एक तत्व के समस्थानिक में होते हैं-
(a) समान भौतिक गुण (b) भिन्न रासायनिक गुण
(c) न्यूट्रॉनों की अलग-अलग संख्या (d) भिन्न परमाणु संख्या
उत्तर-(c) न्यूट्रॉनों की संख्या भिन्न होती है।
प्रश्न 17. Cl-आयन में संयोजकता-इलेक्ट्रॉनों की संख्या है-
(a) 16
(b) 8
(c) 17
(d) 18 उत्तर-(b)8
प्रश्न 18. सोडियम का सही इलेक्ट्रॉनिक विन्यास निम्न में कौन-सा है?
(a) 2,8
(b) 8,2,1
(c) 2,1,8
(d) 2,8,1 b उत्तर-(d)2,8,1
प्रश्न 19.निम्नलिखित सारणी को पूरा कीजिए-
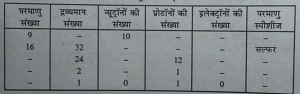
उत्तर-

◆◆◆
